Edgar Tharlindher de Souza Aquino, Lucas
Marques da Silva Araújo e Pedro Henrique
Rodrigues de Souza
Um estudo
observacional prospectivo buscou investigar
como a Síndrome Dolorosa Complexa Regional (SDCR)
evolui pontuando os principais aspectos
prognósticos para o quadro. Para isso,
realizou-se um acompanhamento longitudinal
entre os participantes durante um ano. Os
pesquisadores identificaram fatores iniciais
que se associaram a piores desfechos, como
um maior impacto psicossocial relacionado à
dor, menor apoio social, maior índice de
massa corporal e maior sensibilidade à dor
provocada por estímulos leves. Ao final, a
análise evidenciou que tal evolução está
relacionada a fatores físicos e, também,
àqueles ligados ao bem-estar e ao contexto
biopsicossocial dos pacientes.
A pesquisa
incluiu 113 pessoas que apresentavam SDCR em
fase inicial (há seis meses). Entre os
aspectos relacionados à condição estavam: a
intensidade da dor, alterações físicas,
capacidade funcional e fatores psicossociais
relacionados à experiência da dor. Embora os
resultados mostraram uma tendência geral de
melhora em muitos participantes, o estudo
identificou que uma parte apresentava dor
persistente e limitações funcionais,
indicando que a condição pode se tornar
duradoura em parte dos casos.
O estudo
conclui que a evolução da SDCR é
influenciada por múltiplos fatores que podem
ser identificados de forma precoce e
pontual. Embora muitos pacientes apresentem
melhora ao longo do tempo, uma parcela
significativa mantém sintomas importantes
após um ano. Dessa forma, os resultados
apontam que os fatores físicos e
psicossociais contribuem para o curso da
doença e que a identificação oportuna desses
elementos pode auxiliar na compreensão da
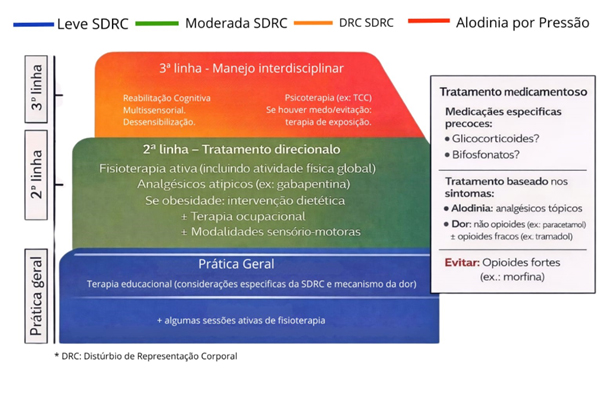
evolução da síndrome. Assim, contribuindo
para o desenvolvimento de instrumentos de
investigação diagnóstica, tais como o
fluxograma que detalha a abordagem potencial
da gestão precoce para o quadro. A partir de
tal ferramenta, direciona intervenções desde
práticas gerais até tratamentos de segunda e
terceira linha, otimizando o cuidado em
saúde.
|
 |
|
Figura 1 (adaptada): Abordagem
potencial de gestão precoce,
estratificada e personalizada
com base nos perfis da SDRC
|
Referências:
-
Louis,
mArc-Henria et al Complex regional
pain syndrome evolution is
determined by both biological and
psychosocial factors: a 1-year
prospective observacional study.
PAIN 167(2):p 396-413, february
2026. | DOI: 10.1097/j.pain.0000000000003815
-
https://journals.lww.com/áin/fulltext/2026/02000/complexregional
pain syndrome evolution is.20.aspx

